Latihan 9
Membuat 2 Soal Pilihan Ganda Per Cahpter
dari Tugas Kelompok Lain (Chapter 19 s/d 25)
Chapter 19
1. Diketahui :
Bila kedua logam tersebut dipasangkan untuk membentuk sel volta, maka pernyataan berikut yang tidak benar adalah …
A. Elektrode Zn teroksidasi dan Elektrode Cu tereduksi
B. Elektrode Zn Sebagai Anode dan Cu sebagai Katode
C. Potensial sel yang dihasilkan adalah 1,10 volt
D. Notasi selnya : Zn(s)|Zn2+(aq)||Cu2+(aq)|Cu E°sel = 1,10 V
E. Dalam sistem sel volta tersebut elektron bergerak dari Cu menuju Zn
Pembahasan :
- Logam yang memiliki E° lebih kecil selalu merupakan Anode (mengalami oksidasi), berarti yang termasuk anode adalah Zn (E° = – 0,76 V) karena memiliki E° yang lebih kecil dari pada Cu (E° = + 0,34 V).
- Karena Zn sebagai Anode maka mengalami oksidasi sedangkan Cu sebagai Katode mengalami reduksi
- Notasi sel volta : Anode|ion||ion|katode
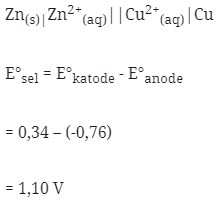
- Dalam sel volta elektron bergerak dari Anode ke Katode berarti dari Zn Menuju Cu, sehingga jawaban yang tidak tepat adalah E.
2. Dalam sel volta elektron bergerak dari Anode ke Katode berarti dari Zn Menuju Cu
A. 1,0
B. 1,5
C. 2,0
D. 3,0
E. 4,0
Pembahasan :
Rumus yang digunakan adalah :
W = e × F
60 = (Ar ÷ biloks Ca) × F
60 = (40 ÷ 2) × F
F = 60 ÷ 20
F = 3
Chapter 20
1. Di antara sifat berikut yang bukan merupakan sifat logam alkali adalah …
A. Terdapat di alam dalam keadaan bebas.
B. Persenyawaannya mudah larut dalam air.
C. Sangat lunak sehingga mudah diiris dengan pisau.
D. Unsur-unsur yang sangat reaktif.
E. Reduktor air yang sangat baik.
Pembahasan :
Logam alkali memiliki sifat-sifat tertentu yang membedakannya dengan unsur kimia lainnya. Sifat tersebut ialah
- pertama logam alkali bersifat sangat reaktif. Sifatnya yang reaktif ini membuat logam alkali tidak pernah ditemukan di alam bebas.
- Sifat kedua ialah memiliki titik leleh yang rendah. Hal itu disebabkan oleh jumlah elektron valensi yang digunakan untuk mengikat partikel lain jumlahnnya hanya satu buah.
- Sifat selanjutnya ialah logam alkali sangat mudah bereaksi dengan unsur kimia lainnya. Mudahnya bereaksi itu disebabkan sifatnya reaktif. Selain itu, logam alkali sangat mudah larut di dalam air.
- Lalu, logam alkali berbentuk padatan, kecuali sesium yang berbentuk cair, dan memiliki karakteristik lunak. Saking lunaknya, padatan logam alkali dapat diiris dengan pisau seperti laiknya lilin atau sabun. Dari penjelasan tersebut, dapat diketahui bahwa jawaban yang tepat untuk soal tersebut ialah A.
2. Beberapa kegunaan unsur/senyawa berikut ini
1. Bahan baku pupuk
2. Peralatan masak
3. Bahan baku semen
4. Menetralisir asam lambung
5. Pembentuk tulang
Kegunaan unsur kalsium atau senyawanya terdapat dalam nomor …
A. 3 dan 4
B. 3 dan 5
C. 2 dan 3
D. 1 dan 2
E. 1 dan 4
Pembahasan :
Kalsium adalah senyawa kimia yang sangat dibutuhkan dalam kehidupan makhluk hidup. Sebab, kalsium memiliki fungsi sebagai tulang dan gigi makhluk hidup, khususnya manusia. Selain itu, senyawa kalsium memiliki fungsi sebagai bahan kimia untuk memproduksi beberapa benda yang digunakan oleh manusia. Benda-benda tersebut seperti kapur tulis, semen, gypsum, dan lain sebagainya. Tentunya, untuk dapat membentuk benda-benda tersebut, kalsium harus digabungkan dengan senyawa kimia lainnya. Dari penjelasan singkat tersebut, sudah diketahui bahwa kalsium berguna untuk tulang manusia dan bahan baku semen. Dengan demikian, jawaban yang tepat untuk soal tersebut adalah B.
Chapter 21
1. Sifat berikut tidak dimiliki oleh golongan halogen yaitu…
A. Unsure bebasnya berbentuk molekul diatomic
B. Titik didih dari atas kebawah semakin besar
C. Merupakan oksidator kuat
D. Mudah bereaksi dengan zat lain
E. Tidak bereaksi dengan air
Pembahasan :
Secara umum, sifat kimia unsur-unsur halogen, antara lain sebagai berikut:
- Umumnya membentuk molekul diatomic, yaitu F2, Cl2, Br2, dan I2
- Mudah bereaksi dengan zat lain. Misalnya, reaksi iodide dengan asam sulfat menghasilkan gas hydrogen sulfide dan larutan triiodida yang berwarna
- Umumnya sukar larut dalam air, namun bereaksi dengan air
- Merupakan oksidator (pengoksidasi) kuat
2. Diantara unsure halogen yang paling reaktif dan yang jauh kurang reaktif adalah….
A. Fluorin dan klorin
B. Klorin dan bromine
C. Bromine dan iodine
D. Fluorin dan iodine
E. Klorin dan iodine
Pembahasan:
Halogen merupakan kelompok unsure nonlogam yang paling reaktif. Namun demikian, kereaktifannya menurun dari fluorin keiodin. Hal itu sesuai dengan keelektronegatifan yang makin kecil dari fluorin keiodin. Fluorin adalah yang paling reaktif, dapat bereaksi dengan hampir semua unsure, termasuk dengan sebagian gas mulia.
Chapter 22
1. Senyawa unsur-unsur transisi periode keempat pada umumnya berwarna. Hal ini disebabkan karena….
A. Orbital d-nya terisi penuh
B. orbital d-nya tidak terisi
C. pengisisan terakhir pada orbital d
D. bersifat paramagnetic
E. Elektron dalam keadaan berpasangan
Pembahasan :
Hal yang mempengaruhi warna ion transisi dalam senyawa adalah subkulit d. Subkulit d memiliki 5 orbital yang masing-masing memiliki tingkat energi yang sama. Apabila ion-ion unsur transisi berikatan dengan unsur ion lain maka muatan listrik anion tersebut akan mempengaruhi 5 orbital d, sehingga terjadi perbedaan tingkat energi antara orbital-orbital d.
Elektron-elektron pada orbital d dapat mengalami perpindahan ke tingkat energi yang lebih tinggi, dengan cara menyerap energi tampak. Besarnya energi yang diserab tergantung jenis atom pusat dan anionnya. Apabila semua energi cahaya tampak diserap maka senyawa tersebut tidak berwarna. Karena orbital d terisi penuh electron atau kosong, maka senyawanya atau ionnya tidak berwarna.
Apabila suatu zat menyerap energi cahaya tampak dengan panjang gelombang tertentu, zat tersebut akan meneruskan cahaya tampak yang tidak diserap mata, sehingga zat akan tampak berwarna sesuai warna cahaya yang diserap.
2. Beberapa reaksi kimia sebagai berikut:
Reaksi yang terjadi pada peleburan besi pada tanur tinggi adalah….
A. 1,2 & 3
B. 1, 2, & 4
C. 2,3 & 4
D. 2,3 & 5
E. 2,4 & 5
Pembahasan:
Pengolahan bijih besi dilakukan di dalam tanur tinggi yang dikenal dengan namablast furnance. Proses pengolahan bjih adalah sebagai berikut.
Bijih besi, kokas dan kapur dimasukkan dari puncak tanur lalu udara panas diembuskan dari bawah. Reaksi yang terjadi pada tanur tinggi adalah sebagai berikut.
“Udara panas yang diembuskan kedalam tanur akan mengalir ke atas dan mengoksidasi kokas dengan reaksi eksoterm menghasilkan gas CO2. Kerika bergerak naik, gas CO2 yang baru terbentuk itu bereaksi lagi dengan kokas yang bergerak turun membentuk CO. Reaksi eksoterm menyebabkan temperature pembakaran di dalam tanur tetap tinggi. Gas CO yang dihasilkan akan mereduksi bijih besi secara bertahap.
Chapter 23
A. Neutron
B. Partikel alfa
C. Partikel beta negatif
D. Positron
E. Proton
Pembahasan:
Berdasarkan pertanyaan di atas dapat diselesaikan dengan :
Jadi partikel X nya adalah partikel alfa.
2. Partikel x adalah suatu…
A. Positron
B. Partikel alfa
C. Neutron
D. Proton
E. Elektron
Pembahasan :
Chapter 24
1. Nama senyawa dibawah yang benar adalah…
A. 4-metil 2-kloro pentana
B. 3-metil 2-kloro pentana
C. 2,4-dikloro pentana
D. 1,4-dikloro 2-metil pentana
E. 1,3-dikloro pentana
Pembahasan :
Langkah-langkah menentukan nama senyawa :
- Mengidentifikasi gugus fungsi
- Memilih rantai induk, yaitu rantai terpanjang yang mengandung gugus fungsi.
- Menuliskan nomor, dimulai dari salah satu ujung dari nomor terkecil
- Menuliskan nama berdasarkan abjad, dimulai dengan nama cabang, kemudian rantai induk
- Apabila ada cabang – cabang sejenis digabung dan dinyatakan dengan awalan di, tri, terta, dan seterusnya
2. Aldehid dan keton memiliki gugus fungsi yang sama, yaitu…
A. gugus hidroksil
B. gugus karbinol
C. gugus karboksil
D. gugus karbonil
E. gugus amina
Pembahasan:
Gugus karbonil adalah gugus dimana ikatan atom C rangkap dua terhadap atom O atau (C=O)
Gugus karbinol adalah gugus dimana ikatan atom C tunggal terhadap atom O atau (C-O)
Gugus hidroksil adalah gugus dimana ikatan atom O dan H atau (-OH)
Gugus karboksil yaitu COO-
Gugus amina yaitu -NH2
Chapter 25
1. Berikut ini yang termasuk polimer alam adalah ….
A. Nilon
B. Teflon
C. Pati
D. Plastik
E. Stirena
Pembahasan :
Polimer Alam adalah polimer yang terdapat di alam, berasal dari makhluk hidup.
Contoh polimer alam dapat dilihat pada tabel dibawah ini:
2. Monomer pembentuk polimer dengan struktur
Adalah ….
A. CH2 = CH2
B. CHCl = CHCl
C. CH2 = CHCl
D. CH3 – CHCl – CH3
E. CH3 – CH2Cl
Pembahasan :
Monomer dengan struktur diatas adalah polimer dari Polivinil Klorida, yang mana monomernya apabila disingkat menjadi :
Pada reaksi ini dinamakan polimerisasi adisi dimana terjadi reaksi pembentukan polimer dari monomer yang berikatan rangkap.















Tidak ada komentar:
Posting Komentar